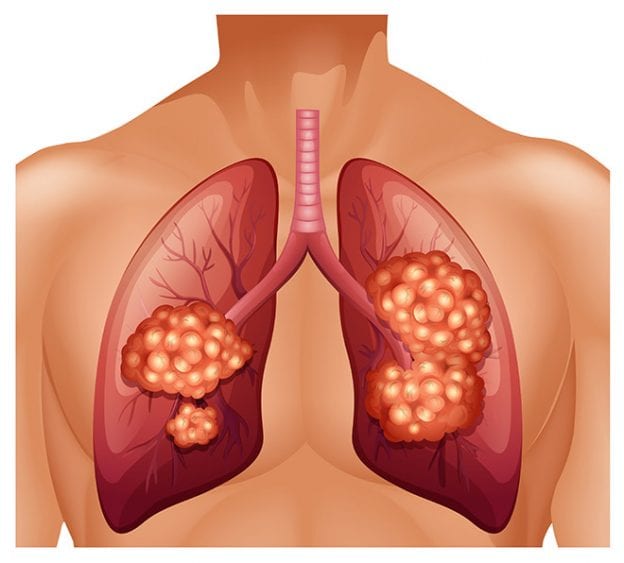
La dependencia de la proteína XPO1
Dado que los genes RAS mutados han estado implicados como factor clave de aproximadamente un tercio de los cánceres, en 2014, el NCI (Instituto Nacional del Cáncer. USA) lanzó una iniciativa especial dirigida a comprender mejor la biología de estos genes y, al hacerlo, fomentar nuevos enfoques para tratar los cánceres alimentados por RAS.
La Iniciativa RAS (que no financió este estudio específico) está apoyando una serie de programas de investigación, incluyendo un esfuerzo recientemente lanzado que está apoyando la investigación para desarrollar nuevos enfoques para identificar relaciones letales sintéticas en cánceres con mutaciones KRAS.
Los investigadores han identificado una debilidad potencialmente crítica en los cánceres de pulmón que tienen mutaciones en el gen KRAS, una alteración genética que promueve el cáncer y que se ha demostrado que es casi imposible de afrontar terapéuticamente. Por otra parte, el equipo de investigación demostró que un fármaco que ya está siendo probado contra otros tipos de cáncer podría explotar con éxito esta vulnerabilidad en las líneas celulares de cáncer de pulmón mutante KRAS y los modelos de ratón con cáncer de pulmón.
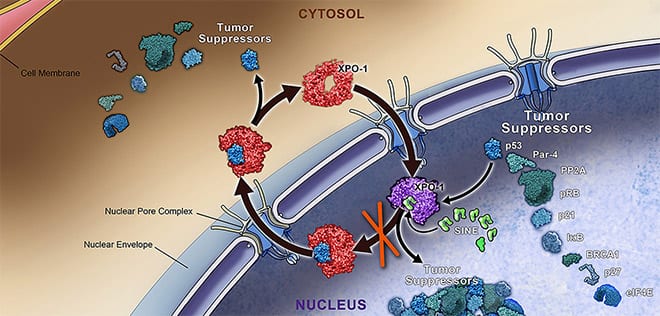
La debilidad radica en la dependencia de las células de cáncer de pulmón KRAS mutante de una proteína, llamada XPO1, que ayuda a lanzar moléculas involucradas en importantes funciones celulares desde el núcleo de la célula en el citoplasma circundante. El inhibidor de XPO1 redujo los tumores en varios modelos diferentes de ratón con cáncer de pulmón de células no pequeñas (NSCLC) -la forma más común de cáncer de pulmón- con mutaciones KRAS.
Los resultados del estudio, indicaron la investigadora principal Jimi Kim, Ph.D., de la Universidad de Texas (UT) Southwestern, y sus colegas, sugieren que «los inhibidores de XPO1 son una estrategia terapéutica prometedora para un considerable grupo de pacientes con cáncer de pulmón».
El estudio fue publicado el 6 de octubre en Nature.
En busca de la letalidad sintética
La familia de genes RAS -que además de KRAS incluye NRAS y HRAS- está entre los oncogenes más estudiados.
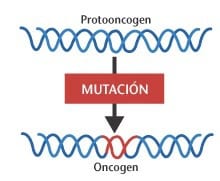
Sin embargo, los esfuerzos para desarrollar terapias que se dirijan directamente a las proteínas mutantes Ras en los tumores han sido obstaculizados por varios factores, incluyendo su compleja biología y sus propiedades estructurales y bioquímicas únicas, explicó Ji Luo, Ph.D., del Laboratorio de Biología del Cáncer y Genética en el Centro para la Investigación del Cáncer del NCI
Las mutaciones en KRAS están presentes en los tumores de aproximadamente el 25% de pacientes con NSCLC. Los pacientes cuyos tumores tienen estas mutaciones suelen tener un mal pronóstico, e incluso si su cáncer responde al tratamiento inicial con quimioterapia, la enfermedad casi invariablemente vuelve. Así que la búsqueda de formas seguras y eficaces para tratar KRAS-tumores mutantes en pacientes con NSCLC es una alta prioridad.
Una forma en que los investigadores están intentando superar la dificultad de dirigirse directamente a las proteínas RAS es buscar un objetivo: identificar y dirigir a los compañeros moleculares o vías de señalización de las que son altamente dependientes para llevar a cabo sus funciones promotoras de tumores. Quita a la pareja, y se crea una reacción en cadena que conduce a la muerte de las células cancerosas, un concepto conocido como «letalidad sintética».
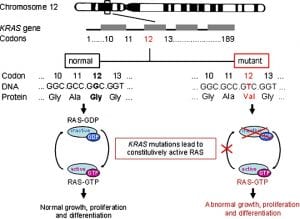
Los investigadores de UT Southwestern utilizaron este enfoque de letalidad sintética en su estudio. Basado en un análisis genómico completo de más de 100 líneas celulares de NSCLC de alta calidad, el equipo de investigación seleccionó las 12 líneas que mejor representaban la composición genómica del NSCLC, explicó el autor principal del estudio, Michael White, Ph.D. Luego, realizaron una «pantalla» letal sintética en estas 12 líneas celulares, desactivando o silenciando sistemáticamente genes para identificar aquellos genes cuya inactivación condujo a la muerte celular en líneas celulares de cáncer que tenían mutaciones KRAS (pero no aquellas con KRAS no mutadas).
A partir de estos experimentos, los investigadores descubrieron que un grupo de genes implicados en el transporte de moléculas fuera del núcleo celular era necesario para la supervivencia de células NSCLC mutadas con KRAS.
Empezando con XPO1
La dependencia de tumores con mutaciones KRAS en estas llamadas proteínas de exportación nuclear llevó al equipo a XPO1. Esto no fue porque la pantalla identificó la XP01 como más importante que otras proteínas nucleares de exportación, explicó el coautor del estudio Pier Paolo Scaglioni, MD, sino porque, por «una afortunada circunstancia», una droga dirigida a XPO1,la KPT-330, ya se ha desarrollado y se está probando como un tratamiento para varios tipos de cáncer.
Los investigadores descubrieron que el fármaco (así como una versión anterior del mismo) mató la mayoría de las líneas celulares de cáncer de NSCLC mutante KRAS y redujo los tumores en diferentes tipos de modelos de ratón de NSCLC mutante KRAS, incluyendo dos modelos que replican de cerca cómo se comporta el cáncer en humanos.
La dependencia del mutante KRAS en el camino de exportación nuclear es «muy inesperada», dijo el Dr. Luo, que no participó en el estudio. El hallazgo, continuó, «ilustra que podría haber otros objetivos no anticipados que pueden ser explotados en los cánceres mutantes KRAS».
El equipo de investigación también identificó por qué la dirección a XPO1 puede causar que las células cancerosas con mutaciones KRAS mueran. Bloqueando la actividad de XPO1, mostraron, se interrumpe una vía de señalización controlada por un factor de transcripción, NF κ B, que afecta la actividad de muchos genes envueltos en promover la supervivencia celular. Al interferir en las señales de supervivencia suministradas por NFκB, el Dr. Scaglioni dijo que las células cancerosas mutantes KRAS mueren pronto.
Pero no todas las líneas de células NSCLC KRAS mutantes y modelos animales respondieron al tratamiento con KPT-330. El equipo de UT Southwestern fue capaz de rastrear esta resistencia a un factor común: una mutación en el gen FSTL5. Esta mutación, encontraron, conduce a la sobreexpresión de la proteína YAP1, otro factor de transcripción que estudios recientes han sugerido puede alimentar el crecimiento del tumor. El bloqueo de YAP1 en líneas de células NSCLC mutantes KRAS, mostraron, podría superar la resistencia al inhibidor de XPO1.
La identificación de mecanismos de resistencia tan pronto como sea posible en el desarrollo de nuevas terapias dirigidas es importante, dijo el Dr. Luo. Citó el ejemplo de los fármacos aprobados por la FDA que se dirigen a tumores con mutaciones en los genes BRAF y EGFR. Aunque muchos pacientes inicialmente responden bien a estos fármacos, la resistencia casi invariablemente se establece.
Así que tener datos sobre la resistencia «puede ayudarnos a estar un paso por delante del tumor», continuó. «Puede ayudar a identificar estrategias potenciales para apuntar a estos mecanismos de resistencia, o prevenir la resistencia de emerger en el primer lugar.»
Pruebas humanas y direcciones futuras
Karyopharm Therapeutics, que desarrolló KPT-330 (también conocido como Selinexor), ya está probando el fármaco en una serie de ensayos clínicos en fase inicial en pacientes con cáncer de sangre y tumores sólidos.
Con base en los resultados de este nuevo estudio en líneas celulares y modelos de ratón, la compañía planea lanzar un ensayo temprano a principios del año que viene probando KPT-330 en combinación con la quimioterapia docetaxel en pacientes con NSCLC avanzado que tiene mutaciones KRAS.
Aunque estos nuevos resultados son importantes y los investigadores están comenzando a hacer algunos avances en el desarrollo de métodos para directamente la meta de RAS, el Dr. Scaglioni dijo que la investigación para identificar socios letales sintéticos para este oncogene común seguirá siendo una prioridad.
El Dr. Luo estuvo de acuerdo, señalando que un enfoque letal sintético tiene importantes ventajas. Al lanzar una red más amplia, continuó, los investigadores pueden identificar más procesos involucrados en la promoción del cáncer «que son inesperados y potencialmente target para una terapia».
Unidad de tratamiento complementario del cáncer de Biosalud Day Hospital
El tratamiento complementario del cáncer de Biosalud Day Hospital nace con la idea de complementar el tratamiento de cualquier enfermedad cancerosa según las técnicas de la Medicina Biológica, potenciando los efectos de la Medicina Convencional y sin efectos secundarios ni contraindicaciones.
Las técnicas que utilizamos son compatibles con los tratamientos convencionales que el paciente esté siguiendo y lo que se pretende es aunar esfuerzos para tener el máximo de posibilidades de superar la situación.
Por eso, siempre estamos al tanto de las nuevas investigaciones sobre el cáncer como ésta, según la cual los inhibidores de la proteína XPO1 son una estrategia terapéutica prometedora para un considerable grupo de pacientes con cáncer de pulmón«.
Fuente: cancer.gov


6 comentarios en «Cáncer de pulmón y mutaciones del gen KRAS»
Me gustaría saber más sobre cancer de olon. Soy paciente de quimioterapia.
Buenos días, este es un blog de información general asociado a la actividad de BIosalud Day Hospital, no es un consultorio online. Le recomendamos que para cualquier consulta, asista a su especialista. Un saludo
buen día, mi padre tiene cáncer de pulmón con mutación Kras, como puedo ofrecerme para el experimento de la terapia dirigida?
Gracias por tu interés en Biosalud Day Hospital. Nuestro equipo médico te enviará en breve un correo electrónico a la dirección de contacto que indicaste.
Hola,
Como el comentario anterior, mi padre también tiene cáncer de pulmón con mutación Kras, como podría participar en vuestro tratamiento?
Saludos,
Catherine
Le recomendamos que se ponga en contacto con nuestro equipo de atención al paciente y nuestro equipo médico a través del formulario de nuestra web https://biosalud.org/contacto/
Los comentarios están cerrados.