
Potenziamento della risposta immunitaria antitumorale con l'ipertermia moderata
L'uso del ipertermia come complemento al immunoterapia del cancro è supportato da un numero crescente di dati di ricerca. I risultati dei dati preclinici e clinici hanno dimostrato una maggiore risposta immunitaria antitumorale con l'aggiunta di un'ipertermia moderata. I meccanismi molecolari responsabili della maggiore riattivazione immunitaria osservata in presenza di ipertermia comprendono la generazione di Hsps (una famiglia di proteine prodotte dalle cellule in risposta all'esposizione a condizioni di stress come lo shock termico), l'attivazione delle cellule presentanti l'antigene e i cambiamenti nel traffico dei linfociti.
L'innalzamento della temperatura corporea è stato riconosciuto fin dall'antichità come una componente benefica della risposta di difesa immunitaria contro gli stimoli patogeni.e l'idea di trattare i tumori umani con il calore risale agli scritti di Ippocrate. Tuttavia, Il calore come modalità di trattamento del cancro ha iniziato a essere valutato in modo rigoroso solo negli ultimi decenni.. C'è un rinnovato interesse per l'applicazione del calore per migliorare l'efficacia delle terapie oncologiche standard, come la chemioterapia e la radioterapia.. La combinazione dell'immunoterapia con l'ipertermia per il trattamento del cancro, tuttavia, è una nozione particolarmente intrigante, in quanto gli effetti clinici significativi dell'ipertermia sono stati attribuiti al sistema immunitario.. La visione accettata dell'interfaccia immunitaria cancro-ospite è che i tumori possiedono antigeni unici che possono essere riconosciuti dal sistema immunitario. Dopo l'assorbimento dell'antigene nei siti tumorali, le APC o le cellule presentanti l'antigene (chiamate anche cellule dendritiche) hanno la capacità di creare una risposta potente entrando nei compartimenti linfoidi e programmando i linfociti. Dopo la generazione e l'espansione a numeri molto elevati, i linfociti citotossici possono raggiungere il sito del tumore per uccidere le cellule cancerose.
Per capire come la temperatura possa influenzare il sistema immunitario, è necessario definire il concetto di ipertermia. Wunderlich, padre della termometria clinica, ha definito la temperatura corporea normale a 37°C e ha descritto un intervallo dinamico di temperature corporee normali con variazioni diurne. La febbre induce l'innalzamento del set point fisiologico della temperatura corporea, aumentando la temperatura corporea centrale attraverso specifici termoregolatori. L'ipertermia differisce fondamentalmente dalla febbre in quanto aumenta la temperatura corporea interna senza modificare il set point fisiologico.. Normalmente, l'ipertermia viene indotta aumentando il carico termico e/o inattivando la dissipazione del calore.

I primi studi sull'ipertermia si sono concentrati sugli effetti citotossici delle alte temperature e sulla morte diretta delle cellule tumorali.. Sebbene sia possibile ottenere una morte cellulare significativa riscaldando le cellule o i tessuti a temperature > 42°C per 1 o più ore, l'applicazione, la misurazione e la coerenza di questo intervallo di temperatura nell'ambito degli studi clinici sul cancro si sono rivelati problematici. A meno che l'ablazione termica del tessuto tumorale non venga applicata in un'area localizzata, L'ipertermia nell'intervallo citotossico non poteva essere ottenuta in modo affidabile in tumori di dimensioni e tipo di tessuto eterogenei. Pertanto, l'ipertermia a temperatura lieve (cioè nell'intervallo della febbre, 39-41°C) e l'ipertermia moderata (41°C) sono emerse come punti focali per le indagini cliniche in corso.in quanto facilmente raggiungibili e tollerati. Ci concentriamo su Hsps e APC e sul miglioramento delle strategie di immunoterapia.
Funzioni cellulari delle Hsps
Le Hsps sono una famiglia di proteine indotte dallo stress con diverse funzioni cellulari critiche e sono tipicamente designate dal loro peso molecolare. Le Hsps sono state scoperte nel 1962 in seguito all'applicazione accidentale di uno stress termico a preparati di Drosophila. Negli ultimi 30 anni, le Hsp sono state caratterizzate in una varietà di cellule, in specie che vanno dai procarioti all'uomo, e sono altamente conservate. Le Hsps attenuano gli effetti dei fattori di stress cellulare. Oggi sono riconosciuti come mediatori centrali di una varietà di funzioni cellulari in condizioni fisiologiche, in quanto sono i principali regolatori dell'attività delle proteine cellulari. Durante l'omeostasi, le Hsp assicurano il corretto ripiegamento post-traslazionale delle proteine e sono in grado di ripiegare le proteine denaturate o di marcare le proteine irreversibilmente danneggiate per la distruzione. Non sorprende che, date le loro attività cellulari cruciali, le Hsps rappresentino uno dei tipi di proteine più abbondanti nelle cellule non stressate, rappresentando 1-2% di tutte le proteine citosoliche. La definizione della funzione delle Hsps nelle cellule tumorali è diventata un'area di ricerca in forte espansione.come descritto di seguito.
Hsps nel cancro
Le attività delle Hsps nelle cellule tumorali trasformate sono complesse e diverse. Le Le Hsps sono presenti in abbondanza in vari tipi di tumori e possono conferire alle cellule tumorali diversi vantaggi in termini di sopravvivenza.. È dimostrato che una specifica Hsp, la Hsp70, inibisce direttamente le vie di apoptosi nelle cellule tumorali, come è stato dimostrato in cellule umane di cancro al pancreas, alla prostata e al cancro gastrico.. Le Hsps sono state anche implicate nel mediare la resistenza all'ipertermia potenzialmente citotossica in un processo chiamato termotolleranza. Più specificamente, la sintesi e l'accumulo di Hsps nelle cellule tumorali esposte all'ipertermia possono fornire protezione contro altri eventi citotossici associati al calore, in quanto le Hsps possono salvare o ripristinare proteine cellulari vitali. La termotolleranza ha la capacità di generare una popolazione di cellule tumorali refrattarie a successivi cambiamenti ipertermici. Inoltre, è dimostrato che le Hsps sostengono il fenotipo maligno delle cellule tumorali, non solo influenzando la sopravvivenza cellulare, ma anche partecipando ai meccanismi di angiogenesi, invasione, metastasi e immortalizzazione. Contrariamente ai numerosi vantaggi conferiti alle cellule tumorali che esprimono alti livelli di Hsps, la dipendenza delle cellule tumorali dalle Hsps per diverse funzioni critiche rappresenta un bersaglio attraente e potenziale per la terapia; un virtuale tallone d'Achille.
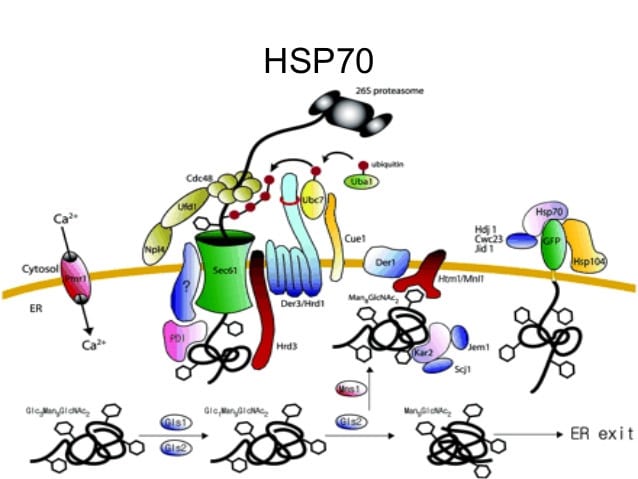
Hsps e sistema immunitario
Il sistema immunitario si è evoluto per sfruttare la capacità delle Hsp di agire come "segnali di pericolo", consentendo la generazione di una risposta immunitaria amplificata.. Le Hsp rilasciate da cellule stressate o morenti attivano le cellule dendritiche (DC), trasformandole in APC mature. L'endocitosi di Hps da parte delle DC aumenta l'espressione sulla superficie cellulare delle molecole MHC di classe II, oltre a diverse molecole co-stimolatorie, migliorando il riconoscimento immunitario degli antigeni. Le cellule dentritiche mature (DC) possono programmare le cellule effettrici dei linfociti in modo limitato all'antigene, limitando così i danni collaterali ai tessuti normali e sani che non esprimono l'antigene bersaglio. La capacità delle Hsps di accompagnare le proteine prima dell'endocitosi e dell'elaborazione da parte delle DC può potenzialmente ampliare il repertorio di epitopi presentati e quindi lo spettro della risposta immunitaria.
Al Day hospital Biosalud abbiamo inserito l'ipertermia nelle nostre tecniche specifiche per il trattamento complementare del cancro, all'interno di un protocollo sviluppato dal nostro dipartimento di R+D+i, aumentando fino a 10 volte l'efficacia delle cellule dendritiche in termini di capacità di distruggere le cellule tumorali, aumentando l'angiogenesi e quindi l'ossigenazione della zona tumorale (l'opposto di ciò di cui hanno bisogno le cellule tumorali) e avviando i meccanismi di apoptosi delle cellule tumorali.
Tutto ciò significa che Il Day Hospital Biosalud può applicare il protocollo più appropriato in modo personalizzato. L'uso di un trattamento che integra la terapia convenzionale prescritta dall'oncologo nel modo più efficace, riducendo notevolmente gli effetti collaterali del trattamento.
Nel cancro, cerchiamo di aggiungere le tecniche complementari che ci offrono le migliori possibilità di successo, data la complessità di ogni caso.

